2026.04.09
【プレスリリース】教科書を書き換える発見! クロマチンの「液体のり」として働くリンカーヒストンH1
概要
ヒトの細胞には全長2メートルにも及ぶDNAが収納されています。これは、ゴルフボールほどの大きさに8キロメートルのひもを押し込むようなものです。いったいどうやって、そんな長いDNAを小さな核に収納し、ギチギチな状態で生命活動を維持しているのでしょうか?この収納に関わる重要な分子が「リンカーヒストンH1」です。分子生物学の教科書では、H1がDNAを規則的にらせん状に折り畳み、30ナノメートル(1)クロマチン線維と呼ばれる「かたい」構造をつくることでDNAを圧縮する、とされてきました。しかし近年、細胞の中にはこのような30ナノメートルクロマチン線維がほとんど存在しないことが明らかになっています。では、H1は本当はどのようにDNAを圧縮しているのでしょうか?
このたび、情報・システム研究機構 国立遺伝学研究所 島添將誠 総合研究大学院大学 大学院生(学振特別研究員DC1)と井手聖 助教(現 東京科学大学 助教)、田村佐知子 テクニカルスタッフ、前島一博 教授のグループは、インド ガンジー工科経営大学GITAMのS. S. Ashwin准教授、京都大学 笹井理生 研究員と共同で、生きた細胞内をナノメートルレベルで可視化できる超解像蛍光顕微鏡(2)を駆使し、生きたヒト細胞の中で、H1のふるまいを観察・解析しました。また、イギリス ケンブリッジ大学のJan Huertas博士研究員、Charles Phillips大学院生、Stephen Farr博士研究員、 Rosana Collepardo-Guevara教授のグループと共同で、分子動力学シミュレーション(3)でH1がどのようにふるまうのかを調べました。
その結果、H1は「液体のり」のようにクロマチン(DNAとタンパク質の複合体)をゆるやかにまとめ、不規則で「やわらかい」構造を作っていることが分かりました。この構造は液体のような流動性をもち、他の分子が入りやすくなっています。つまり、DNA情報の読み出し(転写(4))や複製(5)、修復(6)といった生命活動は、この「やわらかさ」に支えられているのです。
本研究は、教科書を書き換える発見であり、DNAに関わる様々な研究分野に大きなインパクトを与えることが期待されます。また、H1の機能の変化が関係する「がん」や関連疾患の理解につながることが期待されます。
成果掲載誌
本研究成果は、国際科学雑誌「Science Advances」に2026年4月8日(米国東部時間14時)に掲載されます。
研究の詳細
●研究の背景
私たちの体を構成する細胞一つ一つには、全長2メートルにおよぶDNAが収められています。DNAは直径2ナノメートルの細い糸状の物質で、「ヒストン」という樽状のタンパク質に巻き付くことで「ヌクレオソーム」という構造を作ります(図1左)。このヌクレオソームを他のタンパク質と共にさらに折り畳んで「クロマチン」として、細胞に収納するには、「リンカーヒストンH1」(H1)というタンパク質が重要であることが分かっていました。では、H1はヌクレオソームにどのように結合し、どのようにヌクレオソームを折り畳むのでしょうか?
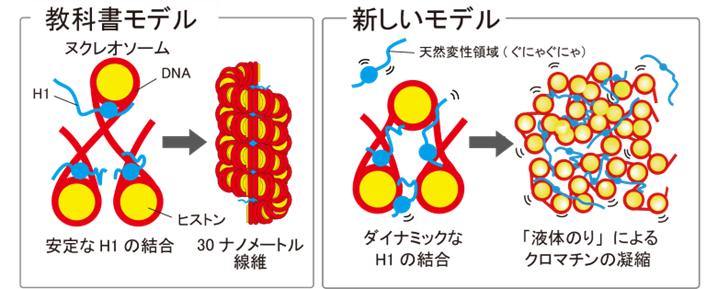
図1:これまで、H1はヌクレオソームの特定の場所に安定に結合し、規則的な「かたい」線維構造を作ってクロマチンを凝縮させると考えられていた(図左)。今回、H1はダイナミックにヌクレオソームに結合し、「液体のり」のように働いてクロマチンを凝縮させ、不規則で「やわらかい」構造を作ることがわかった(図右)。
分子生物学の教科書では、「H1はヌクレオソームの特定の場所に安定に結合し、30 ナノメートルクロマチン線維を形成することでDNAをコンパクトに収納する」とされてきました。30ナノメートルクロマチン線維とは、ヌクレオソームが規則正しく、らせんのように折り畳まれ、線維状になった構造のことです(図1左)。しかし、国立遺伝学研究所の前島教授らは2008年頃より、この30ナノメートル線維は生きた細胞の中にはほとんど存在しないことを明らかにしてきました。教科書のモデルのような30ナノメートル線維が存在しないのであれば、H1は本当はどのようにヌクレオソームに結合し、DNAをコンパクトにしているのでしょうか?
●本研究の成果
本研究では、1個1個のH1分子を観察できる超解像蛍光顕微鏡を駆使し、H1の動きを生きた細胞において観察しました(動画)。その結果、教科書のモデルとは異なり、H1はヌクレオソームに対してダイナミックに結合していることがわかりました。さらに、H1の動きを詳しく解析したところ、H1は不規則に凝縮したヌクレオソームの塊(クロマチンドメイン)の中で、液体のように滑らかに動いていました。この結果から、H1は「液体のり」のように働いて、クロマチンを凝縮させている(DNAを折り畳んでいる)と考えられます(図1右)。
このようなH1の「液体のり」のようなふるまいは、分子動力学シミュレーションでも再現されました(動画)。シミュレーションからは、ひとつのH1分子が複数のヌクレオソームに同時にかつダイナミックに結合することで、ヌクレオソーム同士をゆるやかに繋げて、クロマチンを凝縮させていることがわかりました。
今回明らかになった、リンカーヒストンH1の「液体のり」のような振る舞いは、タンパク質のクロマチンドメイン内部への侵入やドメイン表面上のDNAの移動を促し、凝縮したクロマチンドメインにおける転写(4)やDNA複製(5)、DNA修復(6)などの効率的な反応を可能にすると考えられます。
●今後の期待
本研究では、リンカーヒストンH1が「液体のり」のように働いて、クロマチンを凝縮させていることが明らかになりました。これは教科書を書き換える発見であり、DNAに関わる様々な研究分野に大きなインパクトを与えることが期待されます。また、ある種のリンカーヒストンH1は細胞が「がん」にならないように遺伝子発現を抑えていることが知られています。H1の機能異常は、遺伝疾患にも関連することが知られています。本研究はこれらの関連疾患の理解にもつながると期待されます。
用語解説
(1) ナノメートル
1メートルの10の9乗分の1(10-9)。
(2) 超解像蛍光顕微鏡
通常の光(可視光)を用いた顕微鏡で観察する場合は、200ナノメートル程度の大きさのモノをとらえるのが限界である(光の回折限界)。しかし、超解像蛍光顕微鏡はこの限界を超えて(超解像)、より小さな構造まで観察することができる。本研究では、クロマチンのヌクレオソームをまばらに蛍光標識することで超解像を達成する方法を用いた。
(3) 分子動力学シミュレーション
分子動力学(MD)シミュレーションは、分子や粒子どうしに働く力をもとに、それらが時間とともにどう動くかをコンピュータで計算する方法。実験では見えにくい分子の配置や動きを予測できる。
(4) 転写
DNAに書かれた、細胞の形態や機能を制御する分子の設計図、すなわち遺伝子を見つけ出し、その情報を読み出す反応のこと。読み出された情報をもとに、生命機能を司る特定の分子がつくられる。
(5) DNA複製
細胞が分裂する前に、遺伝情報を2つの娘細胞に引き継ぐために、細胞が持っている1セットのゲノムDNAをコピーして二倍に増やすこと。
(6) DNA修復
DNAが何らかの要因によって切断されたり、DNAの二本鎖がうまく噛み合わなかったりする際に、DNAに書かれた遺伝情報を元通りに直すこと。
研究体制と支援
本研究成果は、国立遺伝学研究所・ゲノムダイナミクス研究室の島添將誠 総合研究大学院大学 大学院生(学振特別研究員DC1)、井手聖 助教(現 東京科学大学 助教)、田村佐知子 テクニカルスタッフ、前島一博 教授、イギリス ケンブリッジ大学のJan Huertas博士研究員、Charles Phillips博士、Stephen Farr博士、 Rosana Collepardo-Guevara教授、インド ガンジー工科経営大学GITAMのS. S. Ashwin准教授、京都大学の笹井理生 研究員との共同研究成果です。
本研究は、日本学術振興会(JSPS) 科研費(JP23K17398, JP24H00061, JP22H00406, JP21H02535, JP22H05606, JP24KJ1161)、武田科学振興財団、UK Government’s Guarantee scheme (EP/Z002028/1): European Research Council (Consolidator Grant)、UK High-End Computing Consortium for Biomolecular Simulation(EP/R029407/1)、Herchel Smith Postdoctoral Fellowship、UKRI Postdoctoral Fellowships Guarantee scheme(EP/X02332X/1)、国立遺伝学研究所NIG-JOINT(4I2023)の支援を受けました。
